- scritto da Riccardo Zerbinati
- categoria Energie rinnovabili
Impianti stazionari ad idrogeno

Durante la prima metà del ‘900 l’intera rete di distribuzione del gas in tutte le città del mondo trasportava un combustibile costituito da gas di cokeria il cui contenuto in Idrogeno superava in alcuni casi il 50% e la rimanente parte era costituita prevalentemente da ossido di carbonio e anidride carbonica, sostituito lentamente negli anni da gas metano.
Un primo ed importante passo, ha portato all’utilizzo di combustibili più puliti e quindi al passaggio da carbone e nafte pesanti, a metano. L’Idrogeno però permette di passare da una ridotta emissione di CO2, a un’emissione pari a zero.
IDROGENO: VANTAGGI E SPERIMENTAZIONI
La grande opportunità che ha oggi l’Idrogeno è legata a due fattori determinanti: il timore che le riserve di combustibili fossili si possano esaurire nel medio periodo, e la necessità di intervenire sulle emissioni di gas serra. I grandi temi di oggi dibattuti riguardo le emissioni inquinanti e il clima alterato, stanno mutando la cultura generale dello spreco e dell’inquinamento.
L’Europa si è posta l’obiettivo di ridurre entro il 2020 il 20% delle emissioni di gas serra, aumentare l’efficienza energetica del 20%, e raggiungere la quota del 20% di fonti rinnovabili per la produzione di energia. Non c’è motivazione migliore per cercare di dare una svolta al sistema energetico.
L’Idrogeno può essere utilizzato per:
- lo stoccaggio di energia;
- il trasporto di energia;
- come vettore energetico non inquinante per la mobilità;
- la capacità di riconvertirsi con l’Ossigeno rilasciando energia elettrica e termica con rendimenti ben superiori a quelli della produzione elettrica convenzionale.
Le realizzazioni con l’Idrogeno non saranno mai appannaggio di un solo attore sul mercato; per far funzionare impianti ad Idrogeno, sono necessarie altre tecnologie che hanno il compito di interagire tra loro.
L’Idrogeno è un gas inodore e incolore (non percepibile dai sensi umani), è classificato come “estremamente infiammabile” dalla normativa sulle sostanze e i preparati pericolosi, con una densità quattordici volte inferiore a quella dell’aria. Per le sue caratteristiche, è il gas con il più alto rapporto energia/peso. Un Kg di Idrogeno contiene lo stesso quantitativo energetico di 2,1 kg di gas naturale, e 2,8 kg di benzina. Il vantaggio dell’Idrogeno è che si diffonde nell’aria a una velocità superiore a quella degli altri gas (perché è il più leggero) ma questa caratteristica è svantaggiosa se si considerano ambienti poco ventilati. L’Idrogeno non è presente in natura allo stato libero, ma la sua disponibilità è pressoché illimitata: ovunque vi sia acqua, c’è anche Idrogeno; la molecola dell’acqua è il composto più diffuso sulla terra. Al contrario dei combustibili fossili, l’Idrogeno è un vettore energetico privo di carbonio; grazie a questa sua caratteristica, durante la combustione, le sue emissioni sono prive di CO2, gas responsabile dell’effetto serra.
Le fonti che possono essere utilizzate per la produzione dell’Idrogeno, sono le più svariate, ma solo alcune, permettono di ottenerlo evitando ogni emissione dannosa (NOX o CO2). Per fonti non rinnovabili, come petrolio o carbone, la produzione di CO2 è sempre presente e va a sommarsi all’anidride carbonica esistente. Anche le biomasse a seguito della combustione, danno luogo a piccole emissioni, in particolare ossidi di zolfo e azoto, e, a seconda della biomassa, anche polveri sottili.
L’utilizzo dell’Idrogeno come carburante per automezzi o come fonte di energie con celle a combustibile o combustori catalitici, è certamente una soluzione valida per sconfiggere l’inquinamento in ambito urbano ma non bisogna dimenticare che per produrre Idrogeno occorre spendere energia elettrica o ricorrere a un combustibile fossile, producendo così inevitabilmente anidride carbonica. L’unico modo per produrre idrogeno evitando le emissioni di CO2, è quello di ricorrere alle fonti rinnovabili che consentono la produzione di energia elettrica, e da questa l’Idrogeno per via elettrolitica. Vi sono ancora alcuni problemi tecnologici da superare per rendere il tutto economicamente conveniente su larga scala. Ultimamente, si stanno spendendo molte energie per studiare una produzione di Idrogeno basata sia sull’utilizzo di fonti rinnovabili, sia sull’utilizzo di combustibili fossili, cercando in quest’ultimo caso di contenere le emissioni di CO2 mediante il confinamento del biossido di carbonio.
Oggigiorno la produzione di questo gas per via elettrolitica, è un metodo molto più costoso di quello derivante dal reforming di fonti fossili ma rimane la sola tecnologia realmente ad emissioni zero e quindi meritevole di molta attenzione e di nuovi sforzi per lo sviluppo di tecnologie basate su questo elemento. Questa modalità di produzione dell’Idrogeno, comporta la scissione dell’acqua in due elementi fondamentali, Idrogeno ed Ossigeno. Non si esclude che l’Ossigeno possa essere utilizzato per altri scopi, ad esempio per quelli ospedalieri. Il consumo di acqua e di corrente per produrre 1 mc di Idrogeno, è circa 5 kWh e 0,8 litri acqua. Contemporaneamente si forma anche un volume di 0,5 mc di Ossigeno. La reazione non può avvenire senza l'aggiunta di un elettrolita nella soluzione e la somministrazione di energia dall'esterno con l'applicazione di un potenziale elettrico agli elettrodi.
Idrogeno per la produzione di elettricitià: Fuel Cells
 fonte www.ttspa.it
fonte www.ttspa.it
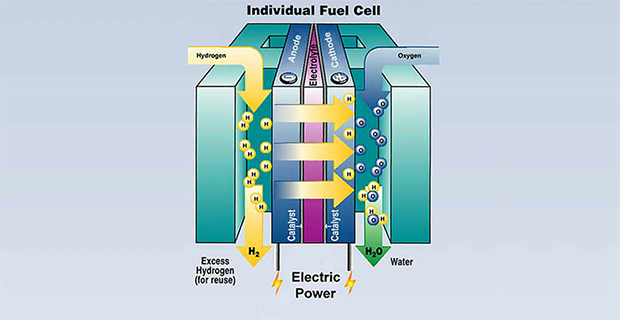
La cella a combustibile è un dispositivo elettrochimico che, come una normale batteria, trasforma energia chimica in energia elettrica, producendo corrente continua. Questa può essere direttamente utilizzata per alimentare un carico elettrico (ad esempio un motore elettrico o un sistema di illuminazione). La differenza principale rispetto ad un normale accumulatore sta nel consumo degli elettrodi, che in questo caso costituiscono solo il supporto sul quale avvengono le reazioni chimiche (riferimento alle Fuel Cell cosiddette PEM “Proton Exchange Membrane”) che sono eterni. Gli elettrodi, un anodo e un catodo, sono separati da un elettrolita, che invece di essere liquido, è una sottilissima membrana polimerica. Questa consente il passaggio solo dei protoni H+ dall'anodo al catodo.
All'anodo viene fornito Idrogeno gassoso puro e, per mezzo di un catalizzatore (platino), viene separato in protoni ed elettroni. A questo punto, mentre i protoni migrano verso il catodo attraverso la membrana polimerica, gli elettroni, non potendo attraversare la membrana, arrivano al catodo passando attraverso un circuito esterno, generando una corrente elettrica.
Al catodo, arriva contemporaneamente anche Ossigeno, che qui si ricombina (sempre con l'aiuto di un catalizzatore, il platino), con i protoni provenienti dalla membrana e con gli elettroni provenienti dal circuito esterno formando acqua. Considerando che una singola cella fornisce ai morsetti una tensione di circa 0,6 V, è necessario collegare più celle in serie, per ottenere la tensione desiderata. Naturalmente ad ogni cella andrà fornito Idrogeno all'anodo e Ossigeno, o aria, al catodo.
Una struttura di celle in serie, è definita “Stack". Oggi esistono degli Stack di celle PEM collegate in serie, costituiti anche da 200 celle. Le singole membrane vengono affiancate una all’altra per produrre più corrente. Durante il funzionamento di una cella a combustibile la sua efficienza non sarà mai, ovviamente, il 100%. L’efficienza media di una FC si aggira sul 50%. Ciò significa che accanto ad una potenza elettrica X ci sarà anche una quantità di calore Y.
È dimostrabile che se tutta l’entalpia di reazione di una FC ad Idrogeno fosse convertita in energia elettrica allora la tensione ai morsetti sarebbe di 1,48 V (se l’acqua prodotta fosse in forma liquida) o 1,25 V (in caso di produzione di vapore acqueo). La differenza tra i valori reali di tensione e quelli ipotizzati rappresenta la quantità di energia trasformata in calore.
L'idrogeno per il riscaldamento delle abitazioni: il combustore catalitico
 Schema di funzionamento del combustore catalitico di Giacomini per l’ossidazione controllata dell’idrogeno, con recupero finale di calore
Schema di funzionamento del combustore catalitico di Giacomini per l’ossidazione controllata dell’idrogeno, con recupero finale di calore
La caldaia a Idrogeno serve per la produzione di energia termica in modo totalmente indipendente dai combustibili fossili e senza produrre emissioni inquinanti.
Il calore viene prodotto dalla combinazione spontanea di idrogeno e ossigeno, ma questi non sono in grado di combinarsi a temperatura ambiente, la reazione chimica ha bisogno di un apporto energetico che si ottiene portando la miscela a circa 180°C. L’evoluzione tecnologica, ha generato combustori che oggi, tramite appositi catalizzatori, sono in grado far avvenire tale reazione anche a temperatura ambiente.
Nel combustore, la reazione catalitica (quindi priva di fiamma) combina Ossigeno e Idrogeno producendo esclusivamente calore e acqua sotto forma di vapore. Il calore prodotto viene prelevato da uno scambiatore integrato nel combustore, e inviato ai circuiti dell’impianto di riscaldamento.
Le regolazioni del combustore eseguite in fabbrica sono protette e possono essere visualizzate e modificate solo da personale autorizzato. Il generatore è dotato inoltre della possibilità di essere comandato dal resto dell’impianto di riscaldamento come una normale caldaia.
È possibile costruire combustori con massimo 6 canali (35 kW).
Impianti con potenze da 5.8 a 17 kW sono ideali per scaldare con efficacia le moderne abitazioni costruite all’insegna del risparmio energetico (classe energetica superiore e riscaldamento a bassa temperatura). La potenza di riscaldamento può essere incrementata con il solare termico.

